近期,南方科技大學化學系副教授何川課題組在“構建雜原子中心手性”領域取得了兩項重要研究進展。相關成果分別發表于國際著名學術期刊《美國化學會志》(Journal of the American Chemical Society,)和《ACS催化》(ACS Catalysis)。
大自然存在大量以碳為手性中心的光學活性化合物,這些碳中心手性化合物在生命的演化進程中發揮了至關重要的作用。有趣的是,作為同一族的硅,以其為手性中心的有機硅化合物在自然界中并不存在。這激發了科學家們創造并研究這一特殊物質的極大興趣。科幻作家甚至大膽推測,與地球的“碳基”生命不同,地外世界可能存在相應的“硅基”生命。近年來,隨著不對稱化學的蓬勃發展,硅中心手性化合物的構建除了傳統的化學拆分、底物手性誘導之外,也逐漸涌現出了一些更為高級的不對稱催化合成方法。與此同時,這些硅中心手性有機硅化合物在合成化學、材料科學、藥物化學以及生命科學等領域也顯示出了非常重要的應用價值。
與碳中心手性相比,sp2雜化的硅原子雙鍵穩定性差,使得通過加成反應來構建硅中心手性的途徑不可行,構建硅中心手性化合物只能依賴于手性拆分或對前手性硅烷的去對稱化。此外,碳–硅鍵的鍵長固有地比碳–碳鍵要長,這就不利于形成緊湊的過渡態;位于第三周期的硅原子可以形成多于四個共價鍵的結構,會因此容易發生硅中心手性消旋化;與硅原子相連的取代基團的結構和性質通常都比較類似,使得其對映面的區分非常困難。以上這些因素都給構建硅中心手性化合物帶了極大的挑戰和難度。因此,如何從簡單的原料出發,通過簡潔、高效、高對映選擇性的方法構建硅中心手性化合物,一直是化學家們研究的一個難點,同時也是推動其在手性功能材料、電子器件、生命及醫藥科學等領域進一步發展應用的基礎和關鍵。
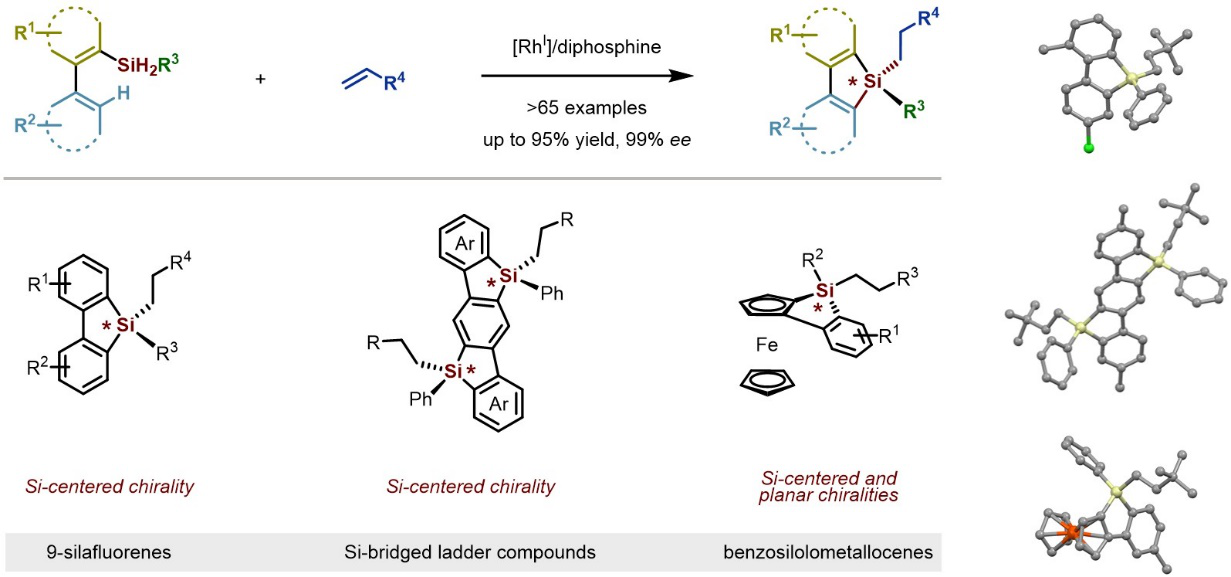
圖1 串聯不對稱碳氫硅化/烯烴硅氫化反應構建硅中心手性
近日,何川課題組從簡單的二氫硅烷和烯烴出發,首次實現了銠催化的串聯不對稱碳氫硅化/烯烴硅氫化反應,“一鍋法”流水線般實現了四取代硅中心手性苯并噻咯類衍生物的高效高對映選擇性構建(Streamlined?Construction?of Silicon-Stereogenic?Silanes?by Tandem Enantioselective?C?H Silylation/Alkene Hydrosilylation, J. Am. Chem. Soc. 2020, DOI: 10.1021/jacs.0c04863)(圖1)。該方法設計巧妙、普適性好,實現了反應化學選擇性、區域選擇性和立體選擇性的完美控制,獲得了一系列含有多種官能團的四取代硅中心手性苯并噻咯類化合物,為結構多樣化的硅中心手性化合物的模塊化合成提供了簡便、高效的新方法。課題組博士后穆德龍和袁偉為論文的共同第一作者,何川為論文的唯一通訊作者,南科大為唯一通訊單位。此外,化學系副教授余沛源在理論計算方面也作出了重要貢獻。
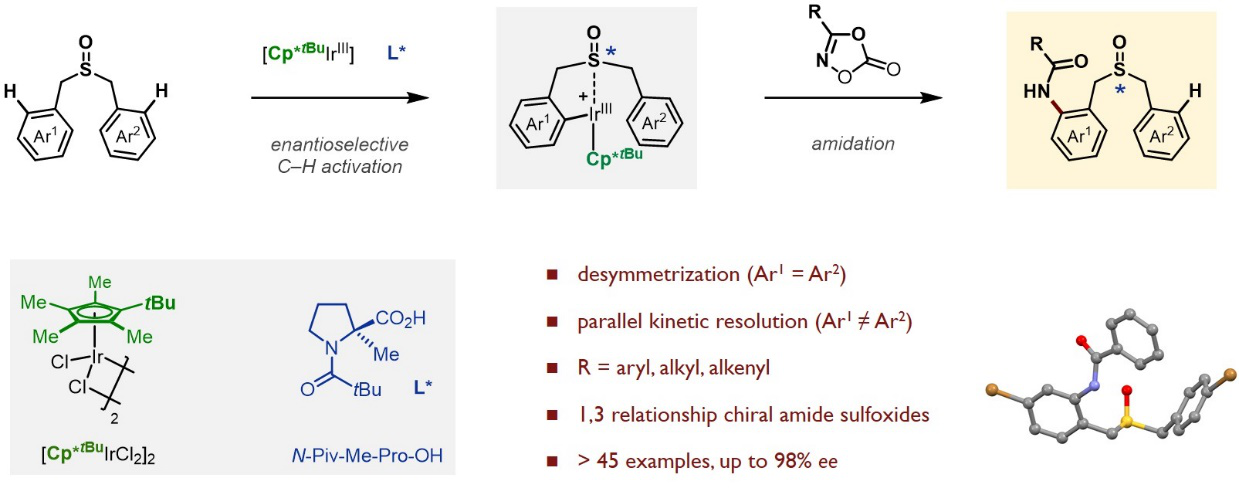
圖2?亞砜導向的不對稱碳氫酰胺化反應構建硫中心手性
除了硅中心手性的構建,何川課題組采用對映選擇性去對稱化和平行動力學拆分的策略,通過對非手性Cp配體和手性羧酸配體的理性設計,發展了Ir(III)催化的亞砜導向的不對稱碳氫酰胺化反應,高效、高對映選擇性地實現了亞砜硫手性中心的構建(Dual-Ligand-Enabled Ir(III)-Catalyzed Enantioselective?C–H Amidation?for the Synthesis of Chiral Sulfoxides,?ACS Catal. 2020, 10, 7207?7215)(圖2)。該方法獲得的手性酰胺化亞砜產物經過簡單的衍生化,可以方便快速地得到一系列雙齒和三齒配體,有望在不對稱催化領域獲得應用。值得一提的是,硫立體中心化合物在新陳代謝中起著非常重要作用;同時,手性亞砜作為一類重要的官能團,廣泛應用于不對稱催化和藥物化學領域。課題組博士后劉文壇為論文的第一作者,何川為論文的唯一通訊作者,南科大為唯一通訊單位。此外,余沛源在理論計算方面也做出了重要貢獻。
以上研究得到了國家自然科學基金委青年項目、深圳市科創委、深圳市諾貝爾獎科學家實驗室項目、相關人才項目經費以及南科大分析測試中心、科學與工程計算中心的支持。
?
發表在《美國化學會志》的論文鏈接:
https://pubs.acs.org/doi/10.1021/jacs.0c04863
發表在《ACS催化》的論文鏈接:
https://pubs.acs.org/doi/10.1021/acscatal.0c02109
供稿:化學系
通訊員:吳笑弟
編輯:程雯璟
主圖設計:丘妍











 魯ICP備2020050029號-1
魯ICP備2020050029號-1 魯ICP備2020050029號-1
魯ICP備2020050029號-1